化学反応式 係数とは 325000-化学反応式 係数とは
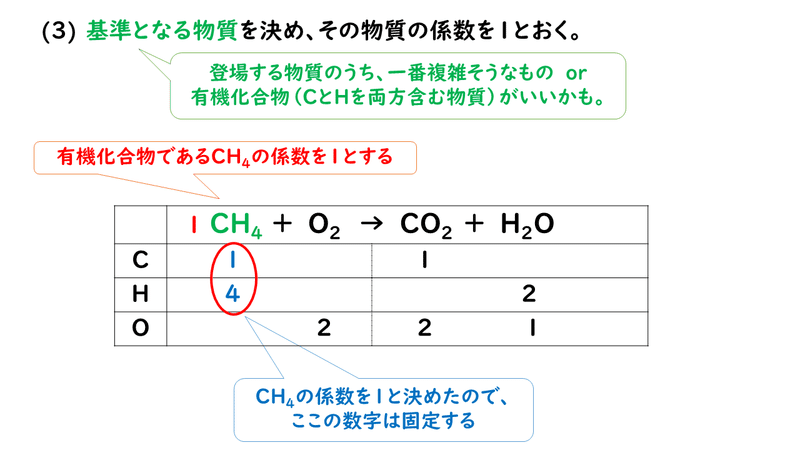
計算式 x 1 CH4 x 2 O2 → x 3 CO2 x 4 H2O C x 1 = x 3 H 4 x 1 =2 x 4 O 2 x 2 =2 x 3 x 4 x 1 = 1 , x 2 = 2 , x 3 = 1 , x 4 = 2C 8 H 18 O 2;化学反応式の係数の比が化学反応における物質量の比を表すことを学ぶ。反応に関与する物質の質量 や体積の間に成り立つ関係を物質量と関連付け,物質の変化量を化学反応式から求めることができる ようになることをねらいとしている。 (2) 生徒観

裏技 未定係数法で化学反応式をつくる方法 理解せずに作れる 化学受験テクニック塾
化学反応式 係数とは
化学反応式 係数とは-全化学反応式においては,中間体を消去して原系と生成 系だけを記すことが通例である。一方,反応速度式には, 律速段階に関係する反応物質だけが現れる。反応速度を規 定している化学反応式と,全化学反応式が異なることがあ る。Ca(OH) 2 H 3 PO 4;




半反応式か化学反応式か 鉛蓄電池の典型問題 化学がちょっとだけ好きな社労士
はじめに ここでは化学反応式について勉強をしていきましょう。 化学反応とは 水を冷凍庫にいれておくと氷に変化します。また、水を沸騰させると水蒸気に変化します。このように物質は同じでも状態が変わる変化のことを物理変化と言います。一方で、あらかじめあ · 化学反応式の基本ルール である 「反応の前後で、原子の数は変わらない」 を使って、係数がアルファベットのまま各原子の数を比べると、方程式ができる。 まず炭素について。 炭素原子は左側にa×6コ、右側にc×1コある。 反応の前後で原子の数は変わらないため、 ・・・① 6 a = c ・ ・ ・ ① 同様に、酸素について、 ・・・② 6 a 2 b = 2 c d ・ ・ ・ ② 水素に · 化学反応式の係数合わせができません。教えてください。コツとかがあれば教えてください! (1)AlO2→Al2O3(2)C3H8O2→CO2H2O(3)H2SSO2→H2OS(4)NH3O2→NOH2Oの4つです。どうしてもわかりません。本当にわがままですみません。 (1)AlO2→Al2O3右辺にAlが2つ、Oが3つあるので、まず左辺のAlの係数を2、Oの
化学反応式の係数は、整数にしなくてはいけません。 分数のままではダメですから、この式の両辺を2倍して、分母を払えば化学反応式の完成となります。 2M 2 O 3 + 6C → 4M + 3CO 2Na 2 S 2 O 3 I 2;係数のつけ方 化学反応式は→の左右で原子の数を合わせることが大事ですが、原子の数が多くなるとモデルではかえって考えにくくなります。 そんなときは数学の連立方程式を使って係数を求めることができます。 例題の手順の③からが今回のテクニックです。 例題4 ブタン( C 4 H 10 ) が燃焼したときの化学反応式を書け。 ①反応前の物質がふくむ原子の
化学反応式の計算を考える際には、 必ず次の三つのことを考えてください 。 反応前の量mol 変化量mol 反応後の量mol mol と表記しましたが、反応式は元々分子の数についての式なので、 質量gなどではいけません 。 必ずmolで考えるようにし(化学変化によって原子は変化したりなくなったりしないから) 化学式の係数は化学式の数を表す。 式の係数は、最も小さな整数にする。 例 4Cu 2O 2 → 4CuO は係数がすべて2で割れるので 2Cu O 2 → 2CuOとなる。 · 目次 1 未定係数法で化学反応式を作るための手順 11 1化学反応に登場する物質の係数を文字式で置く 12 2左辺と右辺で元素ごとに関係式を作る 121 Oに着目 13 31つの文字を1とする(登場回数が多いもの) 14 4文字の答えを元の式に代入し分数を排除



係数を入れて化学反応式を完成させろ 係数が1の場合は1と記せ Yahoo 知恵袋




高校化学基礎 化学反応式の書き方 映像授業のtry It トライイット
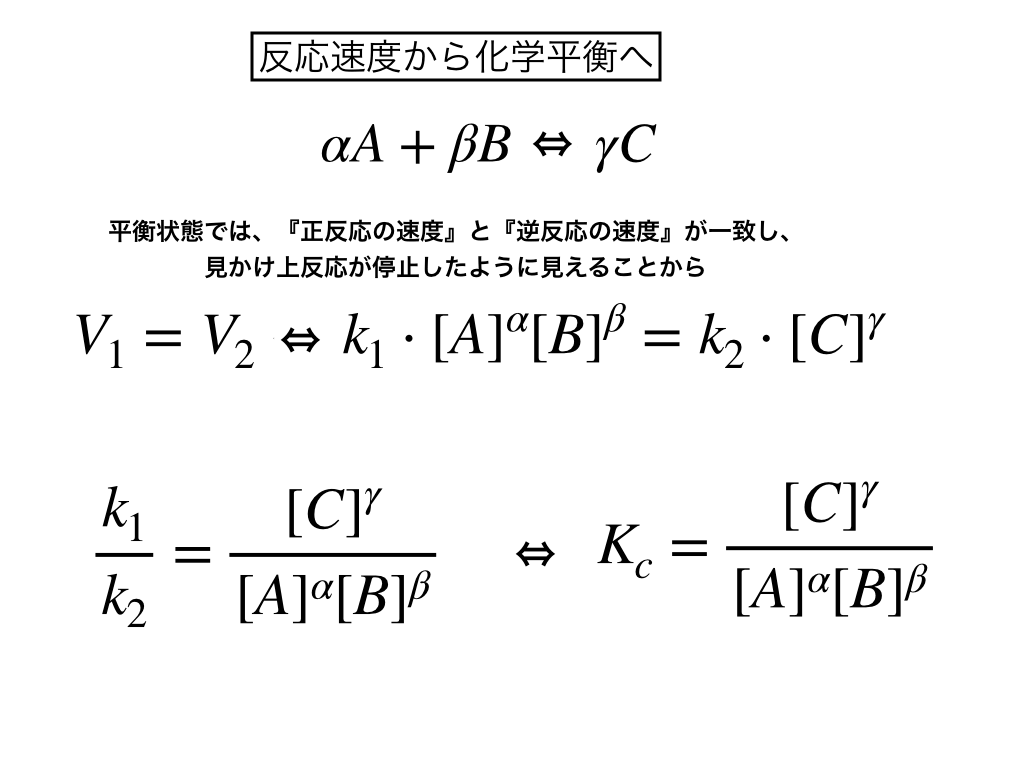
· 高校化学 反応速度と反応式の係数 化学反応の速度の問題で、分からないところがあります。 『水溶液中の物質A、B、Cの間で次の可逆反応が起こり、十分な時間が経過すれば平衡状態が成立する。 この反応の正反応の速度v1は、AとBのモル濃度の積に比例0618 · 一般的に、化学反応式の係数を求める方法としてはじめに習う方法は目算法(他にも呼び方は有ります。 )です。 これは、反応式の左右の分子の係数を過不足ないように"手動"で調整するもの2.化学反応方程式の量論係数の決定と線形空間 化学種は一般に数種の元素がある一定の比率で化合してできており、 元素 A の m mol と元素 B の n mol とから 1 mol の化学種ができる時、 その化学種を A m B n と表記します: * mA nB → A m B n (21) 物質不滅の法則




未定係数法をなるべく使わない 化学がちょっとだけ好きな社労士




化学反応式の係数付けは理解しているのですが イオン反応式はどのようにやればいいのでし Clear
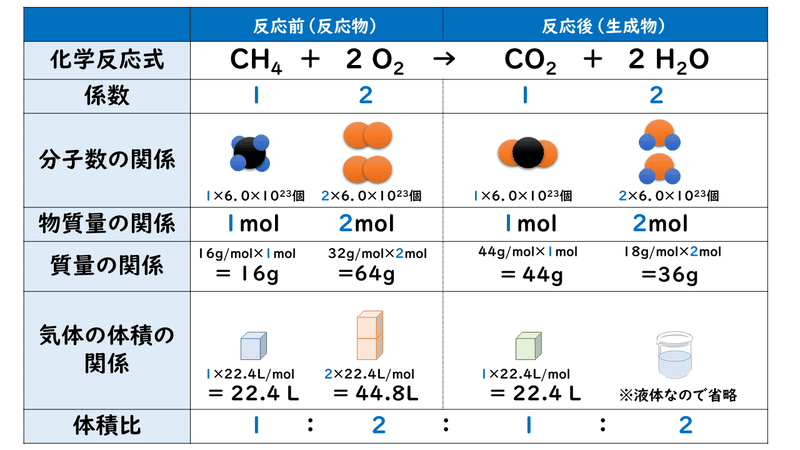
化学反応式の係数の比は物質量〔mol〕の比に一致する。 このことを利用して,化学反応における物質量〔mol〕,粒子数〔個〕,質量〔g〕,体積〔L〕といった量の関係を知ることができる。 CO 10molと反応するO2は,何molか。 反応式の係数比より, CO 2mol と1510 · 今イオンの係数がcuが2+ Alが3+となっていますよね? 反応式は右辺と左辺の電子の量や原子の数が一致していないといけないので、今の場合は2Al+3cu2+→2Al3+ +3cuとなります。 こうすると電子の数は6個でつり合いますし、原子の数もつりあいます!化学反応式の係数の比に着目してみましょう! 2h 2 + o 2 → 2h 2o の分子の数の比は「2:1:2」になっていることがわかります。 この比と気体体積の比が同じになります。(復習:プリント「22原子説と分子説」)



5 2 化学反応の量的関係 1 おのれー Note




イオン反応式の物質についている係数は酸化数に関係あるんですか Clear
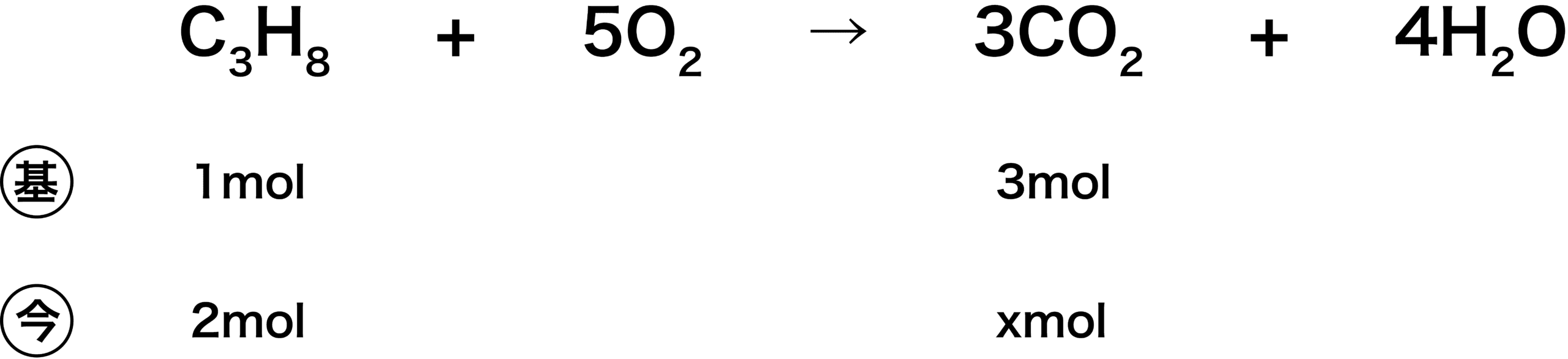
· 化学反応式における係数の比は「molの比」を表している。 例として、次の化学反応式を見てみよう。 N 2 3 H 2 → 2 N H 3 反応式中の係数に注目。 窒素分子(N 2 )・水素分子(H 2 )・アンモニア(NH 3 )の係数はそれぞれ、1・3・2となっている。 この場合、係数から 1molのN 2 と3molのH 2 が反応して2molのNH 3 ができる ということが分かる。 また「係数比=mol比」と11年度「化学」(担当:野島 高彦) モルと化学反応式 0 なぜモルについて理解しなければならないのか なぜモルなどという考え方を理解しなければならないのだろうか? · さて、 係数とは何のこと かというと、 2H 2 + O 2 → 2H 2 O などの化学反応式の の でかこった「2」の部分 (大きい数字)のことだよ。 この化学反応式では、「H 2 」の前と、「H 2 O」の前にそれぞれあるね。 ふーん。 化学式の前につく、 大きい数字のことを「係数」 という んだね



化学反応式 係数 作り方 書き方 計算問題の解き方など 化学のグルメ



5 1 化学反応式 おのれー Note
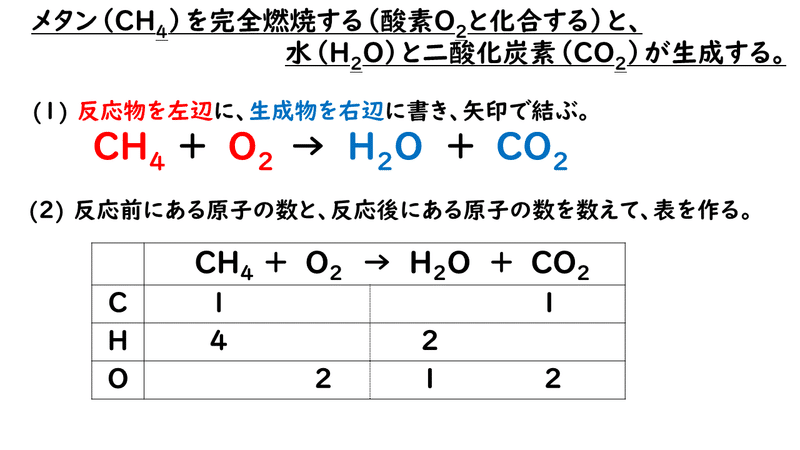
Mg O2 → 2 MgO 炭酸水素ナトリウムの熱分解 炭酸水素ナトリウム→炭酸ナトリウム水二酸化炭素 2 NaHCO3 → Na2CO3 H2O CO2 酸化銅を炭素で還元 酸化銅+炭素→銅二酸化炭素 2 CuO C → 2 Cu CO2 酸化銀の熱分解 酸化銀→銀酸素という化学反応式を例に挙げます。 化学反応式では、 「係数のつけ方」 が特に大事なので 注目してくださいね! (1)まずは、「物質名」と「→」で表す。 水素 + 酸素 → 水 (2)これを、化学式で置き換える。 H₂ + O₂ → H₂O化学反応式の係数より Mg :O 2 = 2:1 の関係なので,Mg 030 mol0 のとき,反応 に必要なO 2= 0150 mol となる。よって,反応せずに残る物資は酸素(O 2)である。 反応せずに残る O 2 の物質量は,0250 mol − 0150 mol = 0100 mol となる。 反応せずに残る O 2




高校化学基礎 化学反応式と係数 映像授業のtry It トライイット




酸化還元反応 電子を含むイオン反応式 化学基礎 定期テスト対策サイト
化学反応式試薬の例(完全な方程式が提案されます): H 2 SO 4 K 4 Fe(CN) 6 KMnO 4;O=C=O O=C=O O=C=O したがって C原子が3個とO原子が6個あることを意味しています。 つまり それぞれの原子の数=係数×それぞれの元素記号の右下の数 (原子数) 5-2-3 化学反応式の係数の求め方 (暗算法) 少し余談ですが、単体で、気体の物質は普通2原子で1つの分子を構成しています。 H 2 , O 2 , N 2 , F 2 , Cl 2, 水素と酸素が反応して、水が生成するときの化学反応式を考え




化学反応 とは何か 反応式が書けるように元研究員が解説 ページ 2 2 Study Z ドラゴン桜と学ぶwebマガジン




化学反応式と物質量




半反応式か化学反応式か 鉛蓄電池の典型問題 化学がちょっとだけ好きな社労士




化学反応式の作り方 ボケのブログ



化学反応式




裏技 未定係数法で化学反応式をつくる方法 理解せずに作れる 化学受験テクニック塾




化学基礎の未定係数法なんですが 110の 2 を過程も含めて教えてくれ 化学 教えて Goo




この問題が解けません 式に係数をつけて化学反応式を完成させます 誰 化学 教えて Goo




高校化学基礎 化学反応式と係数 映像授業のtry It トライイット




化学反応式の係数を簡単に出す方法 おときち副塾長 電脳空間学習塾かもん Youtube




化学反応式の係数を決める 高校 化学 化学基礎 Youtube



反応速度定数の求め方と平衡定数との関係を分かりやすく解説



中2の理科化学反応式なんですが 係数2がつく理由がわかりません Yahoo 知恵袋




高校化学基礎 イオン反応式とは 映像授業のtry It トライイット



3
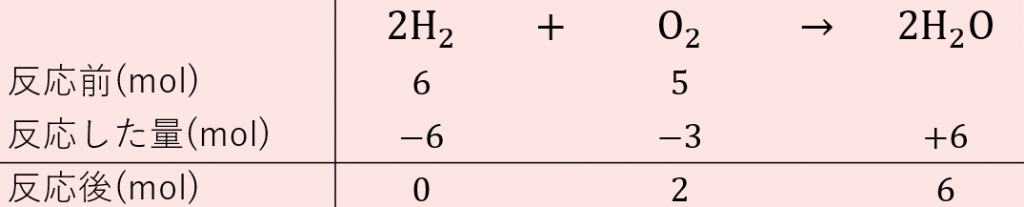



物質量molの超解説 理系ラボ



受験基礎化学 19 化学反応式と物質量 みかみの参考書ブログ




化学反応式の作り方を徹底解説 基礎から複雑な反応まで 高校生向け受験応援メディア 受験のミカタ



化学反応式の係数は分数は不可はルールですか 慣習ですか 分数を Yahoo 知恵袋
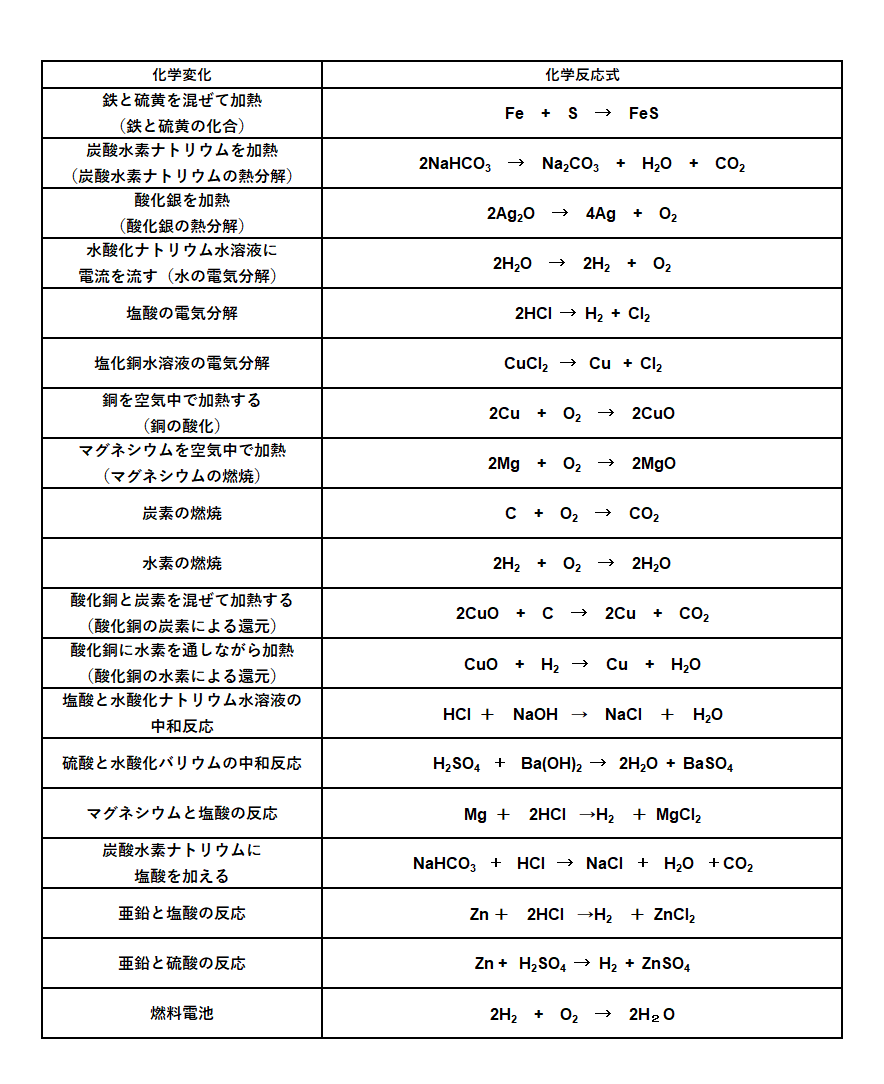



中2化学 化学反応式 中学理科 ポイントまとめと整理




化学反応式と量的関係 過不足が発生するときの反応後の量を求める過程がわかりません 化学基礎 定期テスト対策サイト



受験基礎化学 19 化学反応式と物質量 みかみの参考書ブログ




高校化学基礎 係数と計算 映像授業のtry It トライイット



イオン反応式の係数の求め方がよくわかりません やり方を Yahoo 知恵袋
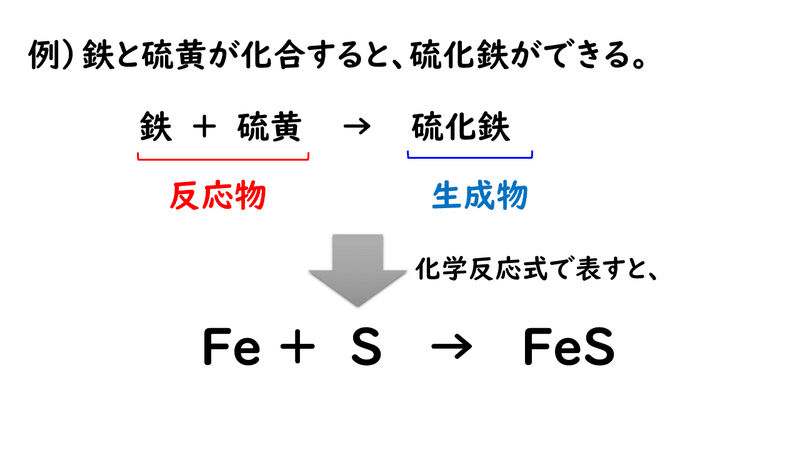



5 1 化学反応式 おのれー Note



イオン反応式の係数の求め方がよくわかりません やり方を Yahoo 知恵袋
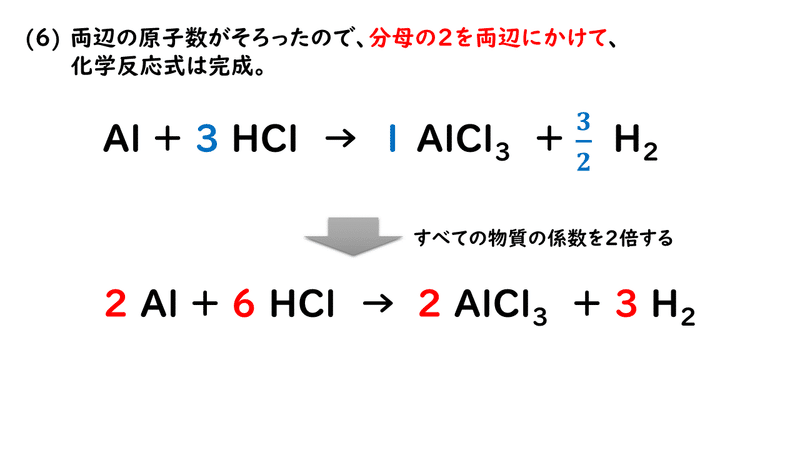



5 1 化学反応式 おのれー Note




化学反応式に係数をつける方法 10 ステップ 画像あり Wikihow




次の化学反応式に係数をつけて反応式を完成させよ ってやつなんです その他 教育 科学 学問 教えて Goo




化学の化学反応式について この問題の一番最後のo2がなぜ3になるのかわか Okwave




化学反応式の作り方 ボケのブログ



1



至急 化学基礎高校一年化学反応式の係数です 助けてください Yahoo 知恵袋



1




化学反応式の作り方を徹底解説 基礎から複雑な反応まで 高校生向け受験応援メディア 受験のミカタ




化学反応式の作り方を徹底解説 基礎から複雑な反応まで 高校生向け受験応援メディア 受験のミカタ




イオン反応式の係数はどうやって求めるのですか 下の問題も教えて 高校 教えて Goo




高校化学基礎 化学反応式と係数 映像授業のtry It トライイット




化学反応式の係数のつけ方が読むだけでわかる




化合と化学反応式 無料で使える中学学習プリント




反応速度定数の求め方と平衡定数との関係を分かりやすく解説
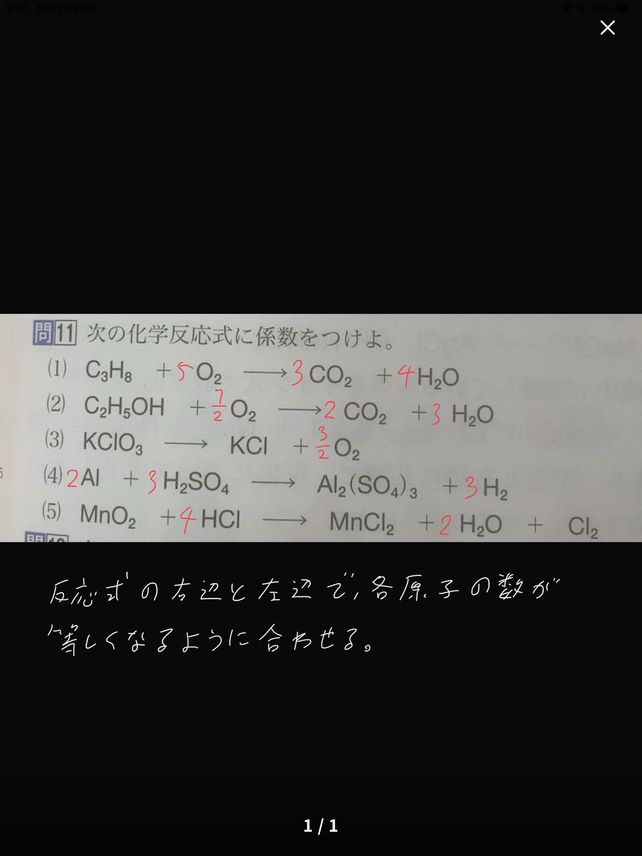



11 1 C 3h8 O2 Co2 H2o Descubre Como Resolverlo En Qanda




Images Of イオン反応式 Japaneseclass Jp




イオン反応式の係数の求め方がわかりません お願いします Clear




中学生の未来のトビラ V Twitter 中学で習う化学反応式は ものすごく少ないので がんばって覚えてください 物質名 化学式 変化 できたら 化学反応式の係数の作り方も覚えておくと化学反応が無限に広がる高校で役に立つと思います 無理だったら高校入試に向けて




化学反応式に係数をつける方法 10 ステップ 画像あり Wikihow



2 o 問1 次の各化学反応式に係数を入れよ



反応方程式の量論係数の決定



反応方程式の量論係数の決定




理科 中2 7 化学反応式の作り方 Youtube




62 1 10 11 O2 Mgo71c Descubre Como Resolverlo En Qanda




Descubre Como Resolverlo En Qanda




化学反応式の係数を決める Youtube




化学反応式に係数をつける方法 10 ステップ 画像あり Wikihow




110 3 4 の解くコツってありますか Clear




化学反応式 Chemical Equation Japaneseclass Jp



化学反応と熱 乙4特訓
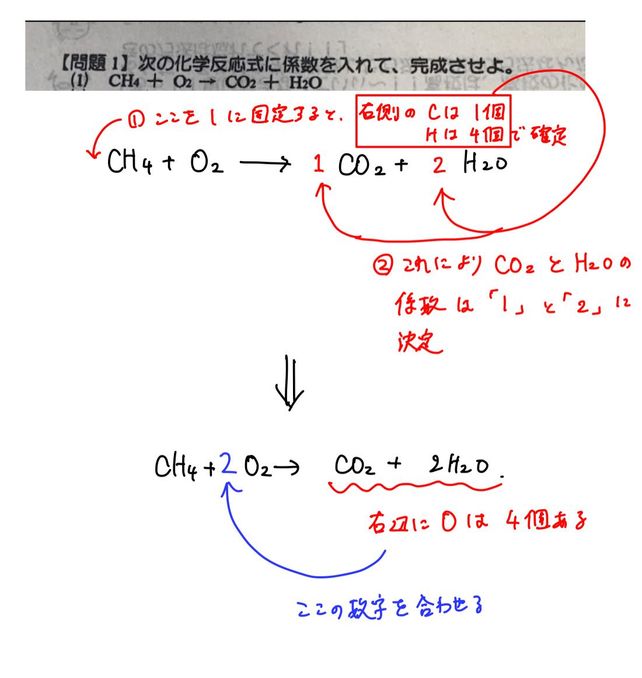



1 Ch4o2 11 00 Descubre Como Resolverlo En Qanda



受験基礎化学 19 化学反応式と物質量 みかみの参考書ブログ



化学基礎の化学反応式の係数の付け方を教えて下さい 写真の化学 Yahoo 知恵袋
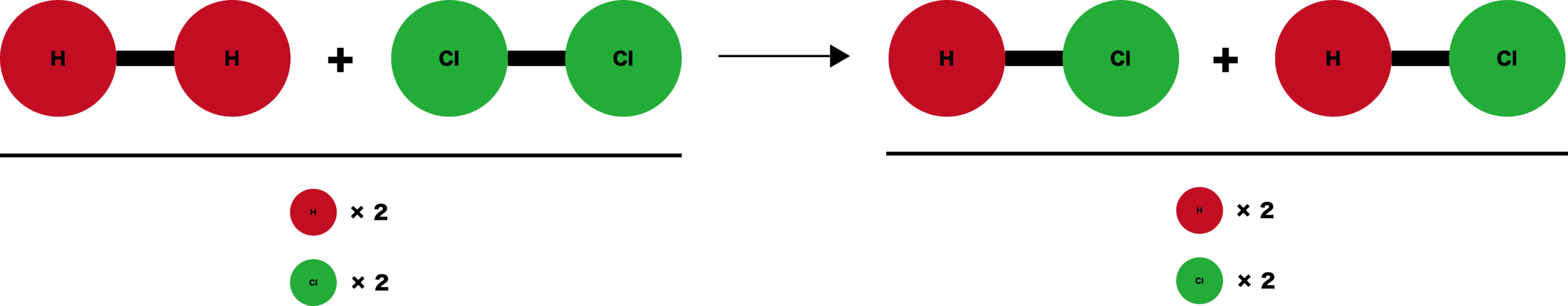



化学反応式 係数 作り方 書き方 計算問題の解き方など 化学のグルメ




イオン反応式 Japaneseclass Jp




改訂化学基礎 改訂化学 ダイジェスト版




化学反応式の書き方を0から解説 その3 係数と式の書き方 Youtube




未定係数法を使い化学反応式の問題やその作り方のコツを身につけよう




化学反応式の係数のつけ方が読むだけでわかる



2 o 問1 次の各化学反応式に係数を入れよ




化学反応式の作り方を徹底解説 基礎から複雑な反応まで 高校生向け受験応援メディア 受験のミカタ
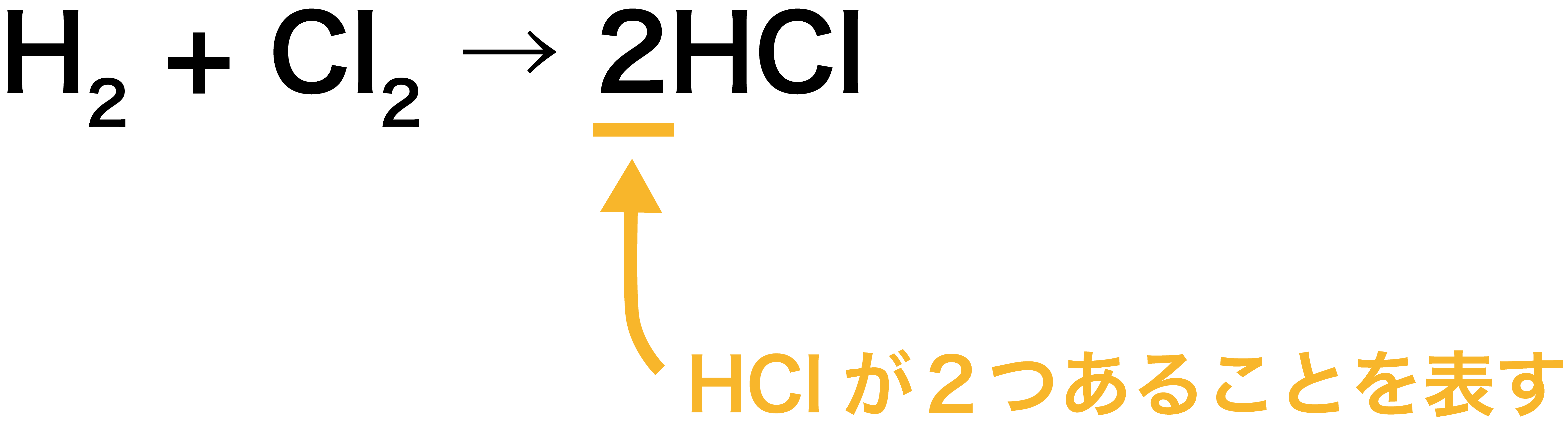



化学反応式 係数 作り方 書き方 計算問題の解き方など 化学のグルメ



化学反応と熱 乙4特訓




Descubre Como Resolverlo En Qanda



化学反応式の係数を答える問題なのですが 6 教えてください Yahoo 知恵袋
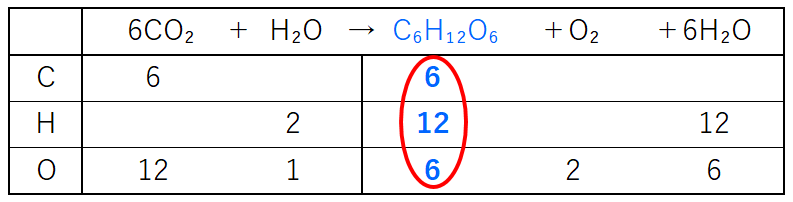



代謝 化学反応式



Http Heian Gacco Que Jp Hannnousiki Pdf




化学反応式の作り方 係数を100 正確に付ける未定係数法を徹底解説




化学反応式 係数 作り方 書き方 計算問題の解き方など 化学のグルメ




今化学基礎で化学反応式をやってるんですけど Clear



5 1 化学反応式 おのれー Note




化学反応式の係数の求め方 教えて下さい 中2です 画像悪くてすみません Clear




高校化学基礎 イオン反応式の書き方 映像授業のtry It トライイット




高校化学 1 7 の回答と 6 7 のイオン反応式の係数の合わせ方を教え 化学 教えて Goo
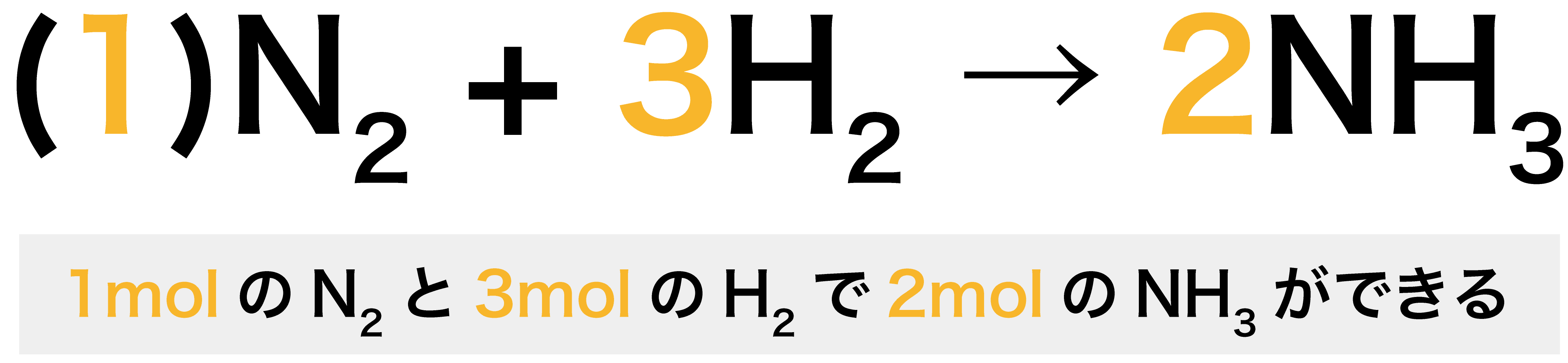



化学反応式 係数 作り方 書き方 計算問題の解き方など 化学のグルメ



1
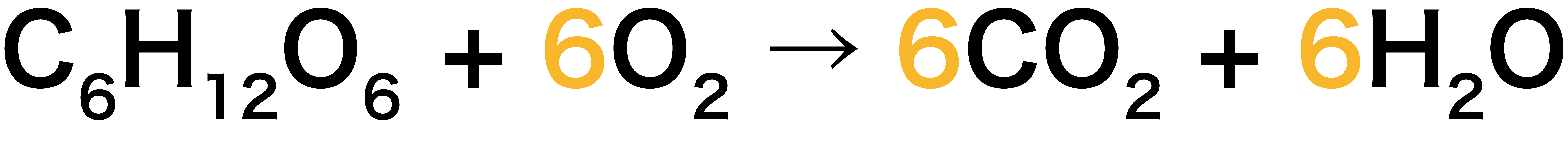



未定係数法 化学反応式の係数を決定する裏技のやり方を大公開 化学のグルメ




5 1 化学反応式 おのれー Note
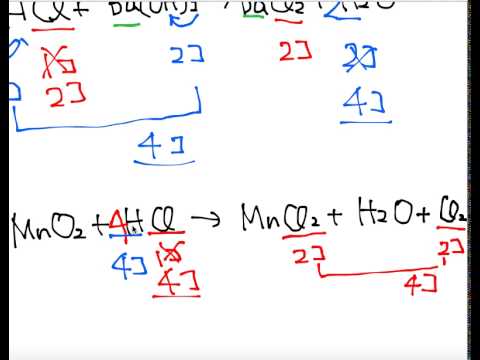



化学反応式の係数 Youtube
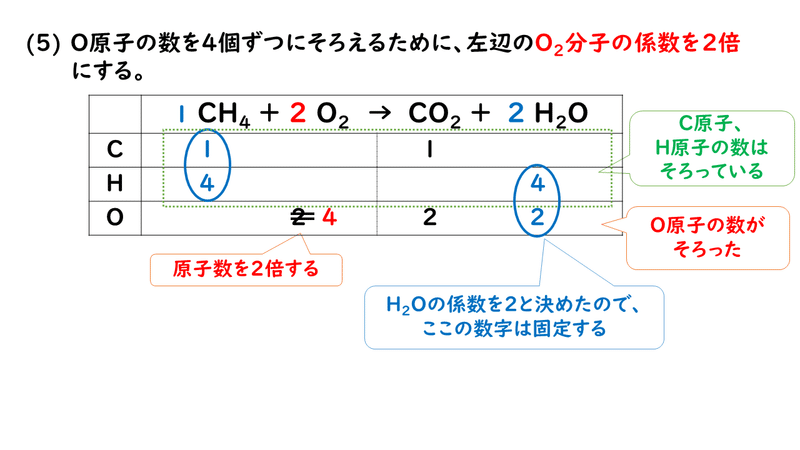



5 1 化学反応式 おのれー Note




化学反応式の係数を合わせる という問題なのですが Clear




化学 化学反応式の係数を決める 未定係数法 Youtube




中学理科 化学反応式の作り方 問題の解き方がわかる3ステップ Qikeru 学びを楽しくわかりやすく




化学反応式と物質量




イオン反応式の係数の求め方がわかりません お願いします Clear




1 Descubre Como Resolverlo En Qanda




改訂化学基礎 改訂化学 ダイジェスト版


コメント
コメントを投稿